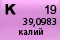
на чём основано:
Периодическая таблица МенделееваОписание:Калий – 19-й элемент Периодической таблицы (заряд ядра 19),
Химический знак – K
Внешний вид простого вещества - серебристо-белый мягкий металл
Атомный номер - 19
Атомная масса - 39,098
Валентность - +1
Плотность, кг/м³ - 860
Температура плавления, °С - 63,6
Теплоемкость, кДж/(кг·°С) - 0,741
Электроотрицательность - 0,8
Ковалентный радиус, Å - 2,03
1-й ионизац. потенциал, эв - 4,34
Структура решётки - кубическая объёмно-центрированная
Природный калий состоит из трёх изотопов. Два из них стабильны: 39K (изотопная распространённость 93,258 %) и 41K (6,730 %). Третий изотоп 40K (0,0117 %) является бета-активным.
В свободном состоянии не встречается. Калий входит в состав сильвина KCl, сильвинита KCl·NaCl, карналлита KCl·MgCl2·6H2O, каинита KCl·MgSO4·6H2O, а также присутствует в золе некоторых растений в виде карбоната K2CO3 (поташ). Калий входит в состав всех клеток.
Применение:- Жидкий при комнатной температуре сплав калия и натрия используется в качестве теплоносителя в замкнутых системах, например, в атомных силовых установках на быстрых нейтронах. Кроме того, широко применяются его жидкие сплавы с рубидием и цезием. Сплав состава: натрий 12 %, калий 47 %, цезий 41 % — обладает рекордно низкой температурой плавления −78 °C.
- Соединения калия — важнейший биогенный элемент и потому применяются в качестве удобрений.
- Соли калия широко используются в гальванотехнике, так как, несмотря на относительно высокую стоимость, они часто более растворимы, чем соответствующие соли натрия, и потому обеспечивают интенсивную работу электролитов при повышенной плотности тока.
Важные соединенияБромид калия применяется в медицине и как успокаивающее средство для нервной системы.
Гидроксид калия (едкое кали) применяется в щелочных аккумуляторах и при сушке газов.
Карбонат калия (поташ) используется как удобрение, при варке стекла.
Хлорид калия (сильвин, «калийная соль») используется как удобрение.
Нитрат калия (калийная селитра) — удобрение, компонент чёрного пороха.
Перхлорат и хлорат калия (бертолетова соль) используются в производстве спичек, ракетных порохов, осветительных зарядов, взрывчатых веществ, в гальванотехнике.
Дихромат калия (хромпик) — сильный окислитель, используется для приготовления «хромовой смеси» для мытья химической посуды и при обработке кожи (дубление). Также используется для очистки ацетилена на ацетиленовых заводах от аммиака, сероводорода и фосфина.
Перманганат калия — сильный окислитель, используется как антисептическое средство в медицине и для лабораторного получения кислорода.
Тартрат натрия-калия (сегнетова соль) в качестве пьезоэлектрика.
Дигидрофосфат и дидейтерофосфат калия в виде монокристаллов в лазерной технике.
Пероксид калия и супероксид калия используются для регенерации воздуха на подводных лодках и в изолирующих противогазах (поглощает углекислый газ с выделением кислорода).
Фтороборат калия — важный флюс для пайки сталей и цветных металлов.
Цианид калия применяется в гальванотехнике (серебрение, золочение), при добыче золота и при нитроцементации стали.
Калий совместно с перекисью калия применяется при термохимическом разложении воды на водород и кислород (калиевый цикл «Газ де Франс», Франция).
Тикер:*K
Автор:Калий (точнее, его соединения) использовался с давних времён. В 1807 году
Г. Дэви электролизом слегка увлажненных твердых едких кали и натра (KOH и NaOH) выделил Калий и натрий и назвал их потассием и содием. В 1809 году
Л. В. Гильберт предложил название "калий" (от арабского аль-кали - поташ.