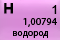
на чём основано:
Периодическая таблица МенделееваОписание:Водород – 1-й элемент Периодической таблицы (заряд ядра 1),
Химический знак – Н
Внешний вид простого вещества - газ без цвета, вкуса и запаха
Атомный номер - 1
Атомная масса - 1,0079
Валентность - (-1), +1
Плотность, кг/м³ - 0,0898
Температура плавления, - °С -259,1
Температура кипения, - °С -252,8
Теплоемкость, кДж/(кг·°С) - 14,442
Электроотрицательность - 2,1
Ковалентный радиус, Å - 0,32
1-й ионизац. потенциал, эв - 13,60
Структура решётки - гексагональная
Водород встречается в виде трёх изотопов, которые имеют индивидуальные названия: протий (Н), дейтерий (D), тритий (T; радиоактивный).
Если кислород является самым распространенным элементом в земной коре, то водород – самый распространенный элемент во Вселенной. Водород составляет около 70 % массы Солнца и звезд. Поскольку водород – наиболее легкий из всех элементов, то такая внушительная масса требует огромного количества атомов этого элемента. Из каждых 100 атомов, встречающихся во Вселенной, 90 – атомы водорода.
Применение:Атомарный водород используется для атомно-водородной сварки.
Химическая промышленностьПри производстве аммиака, метанола, мыла и пластмасс.
Пищевая промышленностьПри производстве маргарина из жидких растительных масел.
Авиационная промышленностьВодород очень лёгок и в воздухе всегда поднимается вверх. Когда-то дирижабли и воздушные шары наполняли водородом. Но в 30-х гг. XX в. произошло несколько катастроф, в ходе которых дирижабли взрывались и сгорали. В наше время дирижабли наполняют гелием, несмотря на его существенно более высокую стоимость.
ТопливоВодород используют в качестве ракетного топлива.
Ведутся исследования по применению водорода как топлива для легковых и грузовых автомобилей. Водородные двигатели не загрязняют окружающую среду и выделяют только водяной пар.
В водородно-кислородных топливных элементах используется водород для непосредственного преобразования энергии химической реакции в электрическую.
Тикер:**H
Автор:Народ